バイアスってなあに?
がん検診の統計値を正しく読み取りましょう!
過去数年で,がん検診については医学界で評価が変化しています.
①検診の回数を多くしても必ずしも癌死は減少しないこと(目的ががんによる死亡の減少なのだから,それが減少しないと意味がないということになります)
②検診によっては,むしろ害があるという新しい理解
がこれらの変化をもたらしています.
検診の評価に関する混乱は,検診研究の結果を導くために用いられる統計の解釈に由来しています.
がん検診を受けた人における生存期間(癌の診断後、患者はどの位の期間生存するか)の改善は,その検診により救命されることを意味するように理解されることが多いですが,いくつかのバイアスがあるため,生存期間や生存率を検診効果の正確な判断に用いることはできないのです.
jnci.oxfordjournals.org/content/102/9/605.long
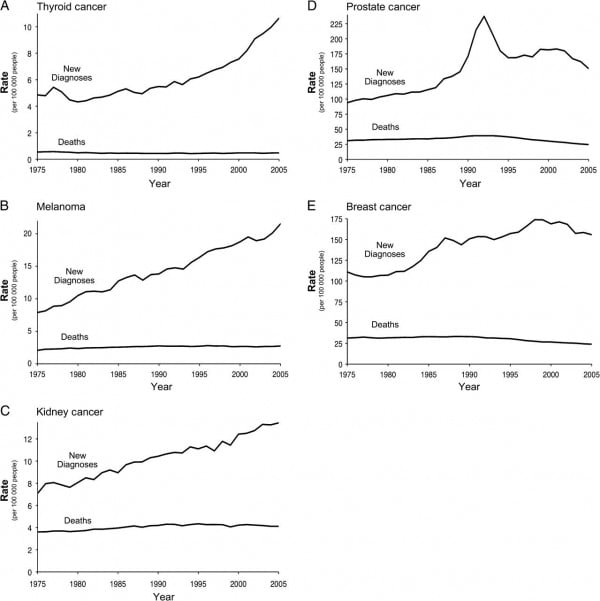
Figure 7
Rate of new diagnoses and death in five cancers in the Surveillance, Epidemiology, and End Results data from 1975 to 2005.A) Thyroid cancer. B) Melanoma. C) Kidney cancer. D) Prostate cancer. E) Breast cancer.
5種類のがんのサーベイランスから新規診断と死亡率をみ
1975-2005年.
A甲状腺がん B悪性黒色腫 C腎がん D前立腺がん
これ.よく見たら,死亡は殆ど変っていません.変わって
過剰診断(放置しても症状も起こさないし死にも至らないがんを,画像新技術の発達などで診断すること)が増えると、罹患率は増えるが死亡率は変わらない
無症状で検査を受ける人の増加,検査の精度の上昇などが過剰診断の原因となります.
過剰診断が増えれば、病気だと診断される人は増える一方,その病気で死亡する人は減りません.
したがって,罹患率は増えるけれども死亡率は変わらない,ということが起こるのです.
経時的に罹患率が増えているが死亡率が変わらない場合は、過剰診断の存在が示唆されるのです.
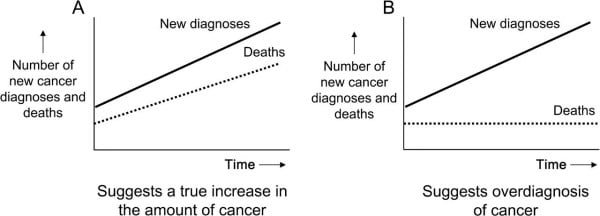
Figure 6
Two distinct patterns of rapid rises in the rate of diagnosis. A) Population data that suggest a true increase in the amount of cancer; B) population data that suggest overdiagnosis of cancer.
左のパターンAの場合は,診断数と死亡数がともに増加しているため,がんそのものが増加しているということです.
右のパターンBの場合は,死亡数は横ばいですが診断数だけが増えています.こういう場合に,過剰診断があるのではと疑われるのです.
疑われる,とお茶を濁すのは,観察研究では他の条件が変わらないことが保証されないためです.
過剰診断がなくても,「罹患率は増えるが死亡率は変わらない」パターンをとることはありえますよね.
①早期発見しても助からない人を検査で見つけるようになると,罹患率は増えるが死亡率は変わらない.
②放置すれば死亡の原因となる癌が実際に増加してるのであるが,治療法の進歩や早期発見によって死亡率が低下している
③経過の長い癌の場合.早期発見によって死亡率が低下するとしても,その効果はすぐにはあらわれません.放置すれば10年後に死亡する癌を,早期発見・早期治療で死亡を回避すると,罹患率はすぐに上がるが死亡率が下がるのは10年後となります.これをタイムラグといいます.
医師たちは,きっと,「早期発見して早期治療することで,がんの治療成績は格段に向上した」という,②の場合を主張するのでしょう.
しかし,②の場合は,真の増加の効果と治療成果による死亡率低下の効果が一致しなければなりません.
そうです.グラフは,図6の右側ではなく,左側のようにならないといけないのです.
しかし,その上の図7を見ると,とてもそのようなグラフには見えませんよね.
よく,「医師からもう1か月遅かったら助からなかったと言われた」なんて話を聞きますし,
川島なお美さんだって,見つかってすぐに手術していたら助かったといっている人たちもいますが
本当でしょうか?????
根拠を出してほしいですよね.科学的根拠を.
ここで,バイアスという言葉を理解しないといけません.
www.med.osaka-u.ac.jp/pub/kid/clinicaljournalclub14.html
こちらから引用します.
臨床研究の基本的な目標は、exposureとoutcomeの関係の強さを検討する事です。バイアスとは、exposureとoutcomeの関係の強さを系統的に歪めてしまうものであり、一般的に選択バイアス、情報バイアス、交絡に分類されます。それぞれのバイアスが、実際に臨床研究が進められているステップのどこに深く関与しているかに注目すると、理解しやすいです。

選択バイアス(selection bias)
臨床研究の第1段階は、研究の対象となるtarget population(目的母集団)を設定し、target populationの中からsample(標本)●をランダムに抽出する事です。選択バイアスが存在すると、target populationからのsampleの抽出がランダムに行われず、target populationとsampleの間にズレ(歪み)が生じてしまいます。
実に様々な種類な選択バイアスが存在しますが、下記はその一部です。
Survivor Treatment Selection Bias
生存期間が長い症例ほど、治療介入を受けやすい。
Referral Filter Bias (Healthcare Access Bias)
予後不良例や治療抵抗例が専門施設に集積する。
Length-bias Sampling
疾患罹患期間の長い症例(=予後良好例)が研究対象にされやすい。
情報バイアス(information bias)
臨床研究の第2段階は、target populationからランダムに抽出された標本のデータを収集する事です。情報バイアスが存在すると、収集されたデータに歪みが生じてしまいます。
実に様々な種類な情報バイアスが存在しますが、下記はその一部です。
Observer/Interviewer Bias
対象症例のexposureやoutcomeの情報が先入観となり、データ収集に影響を与えてしまう。
Reporting Bias
飲酒歴や喫煙歴の自己申告は、過小申告の傾向がある(underreporting bias)。
Lead-time Bias
スクリニーング群の方が、疾患が早期発見されるため、非スクリニーング群よりも疾患罹患期間が長くなる(=予後良好である)。
交絡(confounding)
臨床研究の第3段階は、収集されたデータを解析することによって、exposureとoutcomeの関係の強さを評価する事です。交絡因子とは、exposureにもoutcomeにも関連している因子です。したがって、交絡因子の存在を考慮しなければ、expoureとoutcomeの関係を過大評価あるいは過少評価してしまいます。

例えば、解析の結果、飲酒(expoure)と末期腎不全(outcome)の間に強い関連性が認められたとします。しかしながら、飲酒習慣のある人には、喫煙している人が多いため、末期腎不全を発症しやすいかもしれません。あるいはメタボリック症候群の人が多いため、末期腎不全を発症しやすいのかもしれません。喫煙とメタボリック症候群は、飲酒とも末期腎不全とも関連している交絡因子なので、飲酒(exposure)と末期腎不全(outcome)の関係を検証するためには、交絡因子である喫煙とメタボリック因子の存在を考慮しなければなりません。
バイアスの調整方法
バイアスを調整するために方法は、研究デザインを立案する時点で制御する方法と、データ収集が終了した後に統計学的手法を用いて制御する方法があり、バイアスの種類によって異なります。
| バイアス | 研究デザイン | 統計解析 |
|---|---|---|
| 選択バイアス | ○ | × |
| 情報バイアス | ○ | × |
| 交絡 | ○ | ○ |
選択バイアスと情報バイアスは、研究デザインを立案する時点で制御しなければならず、データが収集された後に調整することができません。
一方、交絡は、研究デザインを立案する時点で制御したり、あるいは統計解析の時点で調整する事も可能です。
したがって、バイアスを調整するために最も重要なことは、データ収集を開始する前段階である研究計画を立案する時点で、バイアスの制御を考慮した研究デザインを立てる事です。
参考文献
Delgado-Rodriguez M, Llorca J. Bias. J Epidemiol Community Health 2004; 58:635-641
それでは,検診について考えてみましょう.
症状による癌診断の前に,検診によって癌が早期に発見されると,リードタイム・バイアスが生じるのですが,早期診断によって疾患の経過が変わることはありません.
たとえば,55歳でがんができて,67歳で症状を発症してがんと診断されて3年後に70歳で死亡した人を考えてみましょう.
5年生存率はゼロ.
しかし同じ人が,62歳で検診で症状の出る前に発見されると,5年生存率は100%となります.
リードタイム・バイアスは,発見後の生存期間を比較するすべての解析に伴うものです.
このため,早期診断による癌発見後の5年生存率は,検診により救命が可能かどうかを判断するには大変不正確なものとなります.
残念ながら,発見後の寿命が延びるという認識が医師たちにきわめて強い可能性があるのです,
落ち着いて,こういう統計学的数字を理解するセンスを身に着け
医学の常識が明日は非常識となる可能性を認識し,常に批判的検討を加える,という姿勢を持たねばなりません.
常識,というのは,いつでも覆る可能性を秘めています.
当然でしょ.
当たり前でしょ.
そんなものは,世の中に何一つない.私はそう思っています.
#新宿ミネルバクリニック #がん専門医 #在宅 #仲田洋美 #緩和 #セカンドオピニオン #セカオピ #がん治療 #放射線 #遺伝子検査 #認知症 #近藤誠 #在宅緩和ケア #緩和ケア
#検診 #早期診断 #早期治療 #川島なお美

コメント